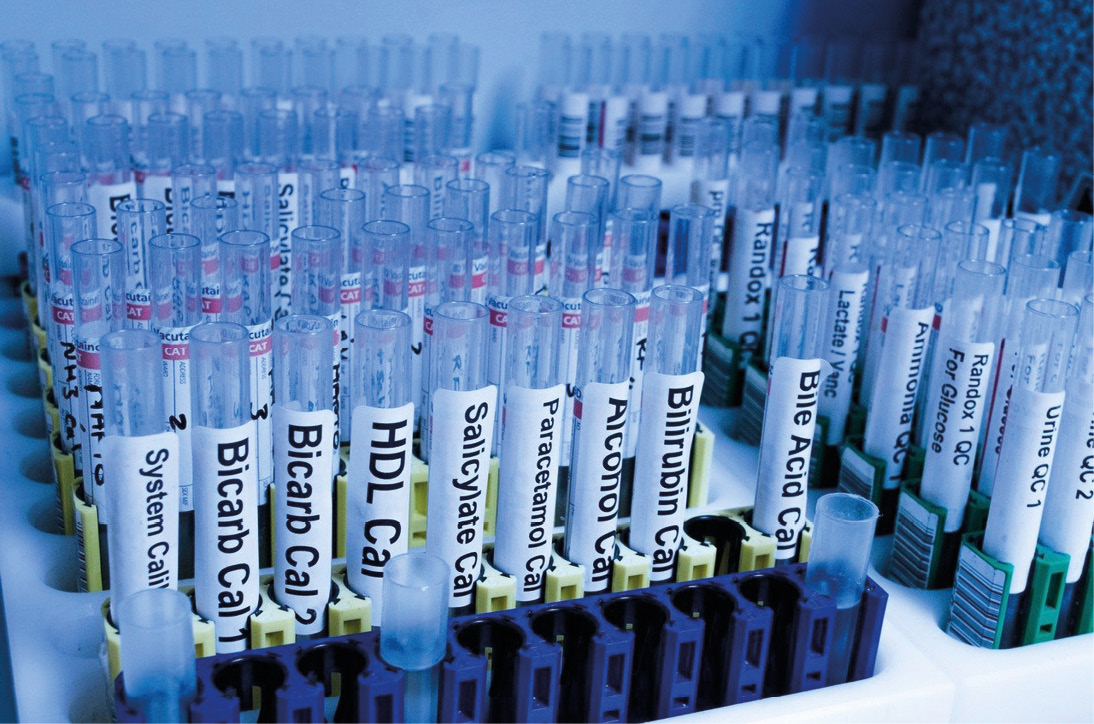
La toxicología desde la antigüedad
Desde la antigüedad, el humano ante su necesidad de alimentarse experimentó efectos tóxicos con el uso de ciertas plantas, animales y minerales, que lo llevó a generar un conocimiento empírico relacionado con las sustancias venenosas. De acuerdo con las evidencias históricas, se utilizaron sustancias tóxicas desde el Paleolítico, donde se reporta el uso de venenos como arma para la caza, en la guerra, en la medicina o en el envenenamiento intencionado, lo que dio lugar al surgimiento del término toxicología.
Durante la edad de Bronce, se utilizaba el fruto de la adormidera (Papaver somniferum) para impregnar los extremos de las flechas, además de venenos de araña, serpiente y otros animales, los que han sido descritos en el papiro de Hearst. En el libro de los Vedas y en la Biblia (1500 años antes de nuestra era), se citan ejemplos de eméticos y la fórmula de un antídoto: «Moisés da instrucciones en la Biblia, sobre cómo proceder con los utensilios de cobre donde se cocinaba, para evitar posibles intoxicaciones por el acetato de cobre».
En el Papiro de Ebers escrito 1500 años antes de nuestra era, se presenta información de forma explícita sobre el carácter venenoso de plantas como Papaver somniferum, Aconitum napellus, Hyoscyamus niger, Helleborus argutifolius, Conium maculatum, Cannabis indicus y de metales tóxicos como el plomo, arsénico, antimonio y cobre. Además, también contenía instrucciones para la preparación de sustancias para provocar abortos.
¿Qué es toxicología y por qué es esencial para el desarrollo de medicamentos?
Hoy día, la toxicología va más allá del estudio de los venenos y es considerada una herramienta esencial para el desarrollo de medicamentos. Después del desastre de la talidomida®, un fármaco desarrollado por Química Grünenthal, que ocasionó el nacimiento de niños con amelia (ausencia de toda extremidad), focomelia (pérdida o acortamiento grave de los elementos proximales) y ausencia/hipoplasia del pulgar o de los dedos, la evaluación toxicológica de nuevos candidatos terapéuticos se convirtió en una etapa ineludible del desarrollo farmacéutico.
La toxicología, como su nombre lo indica, estudia diversos aspectos relacionados con la acción tóxica de un fármaco, desde la evaluación de la absorción, distribución, biotransformación y excreción del candidato terapéutico y de sus metabolitos (toxicocinética), hasta las interacciones moleculares sobre dianas o los blancos toxicológicos (toxicodinámica), que pueden conducir a respuestas adaptativas, de tolerancia, reparación y daño parcial o total.
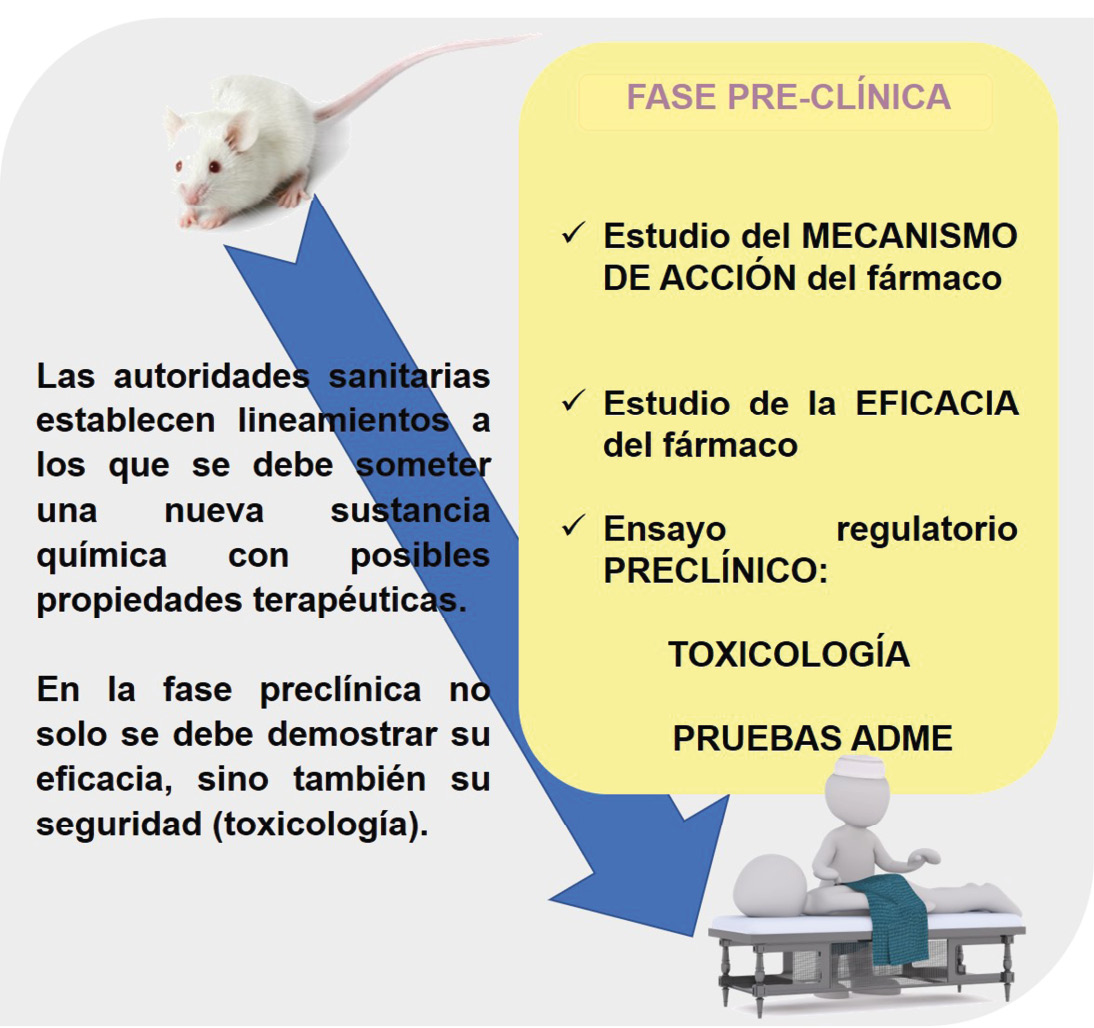
La evaluación toxicológica de los nuevos fármacos se realiza en animales (fase preclínica) y en seres humanos (fase clínica). A nivel preclínico pueden realizarse las siguientes pruebas: toxicidad aguda (efectos de dosis únicas); subaguda y crónica (efectos de dosis múltiples durante tiempos prolongados); efectos sobre el comportamiento reproductivo (conducta de apareamiento, reproducción, preñez, parto, descendencia, teratogénesis y defectos congénitos); potencial carcinogénico, mutagénico y otras.
Para ello, se considera la determinación de índices toxicológicos como la NOAEL (dosis sin efecto adverso observable), la LOAEL (menor dosis que produce un efecto adverso), y la DL50 que representa la dosis que provoca la muerte al 50 % de los individuos en experimentación. Estas pruebas son aplicadas sobre animales para el conocimiento de las dosis efectivas y letales que ayudan a determinar el margen terapéutico, definido como la relación entre la dosis del fármaco que produce el efecto terapéutico y la que provoca el efecto tóxico. Los estudios toxicológicos preclínicos permiten realizar análisis rigurosos de eficacia y seguridad del nuevo candidato, antes de su uso en seres humanos (Saber Más, 9(50):57-59). Además, se realizan las pruebas ADME, que evalúan la absorción, la distribución, el metabolismo (biotransformación) y la eliminación de los fármacos en los procesos de la farmacocinética.
Durante la fase I de investigación clínica, realizada en sujetos sanos o en algunos casos en pacientes, se sigue estudiando la seguridad del medicamento y se decide la pauta de administración para ensayos posteriores. Durante las fases II y III, se recaban evidencias de la eficacia y se responden preguntas cruciales sobre la seguridad del fármaco y su utilidad terapéutica a través de un monitoreo exhaustivo de los pacientes. Durante la fase IV o de post-comercialización, se llevan a cabo estudios de farmacovigilancia, incluyendo la detección de eventos adversos y estudios de morbilidad y mortalidad. Así, aunque el fármaco esté en el mercado, su evaluación toxicológica no cesa, sino que este monitoreo continúa para garantizar la seguridad de los pacientes.

Impacto de la bioética en los estudios toxicológicos
Como ya se explicó, la toxicología preclínica regulatoria requiere el uso de animales de experimentación. La bioética animal surge como consecuencia de reconocer los derechos de estos. Es así como los comités de bioética en varios países del mundo, han promulgado normas y reglamentaciones que conducen a la coordinación y supervisión de los procedimientos dirigidos al cuidado y manejo de los animales sometidos a experimentación toxicológica.
Con la introducción de los nuevos métodos toxicológicos alternativos, han surgido recientes variantes para la estimación y evaluación de las características tóxicas de una sustancia, mediante métodos alternativos que siguen el principio de las tres R: reducción, refinamiento y reemplazo. La primera se refiere a la reducción del número de animales empleados en cada ensayo, mientras que la segunda está relacionada con refinar procedimientos existentes para disminuir el sufrimiento de los animales. En el reemplazo, se propone la utilización de modelos in vitro, en especial cultivo de células, protozoarios, bacterias y modelos computacionales en lugar de animales de experimentación.
El empleo de animales de experimentación debe estar respaldado por un protocolo de ensayo, que se confecciona cumpliendo las Normas Internacionales y Buenas Prácticas de Laboratorio (BPL) no clínicas y los protocolos específicos del estudio. En México, la Norma Oficial Mexicana 062 (NOM-062-ZOO-1999) establece las especificaciones técnicas para la producción, cuidado y uso de los animales de laboratorio.
La toxicología moderna
En la actualidad, la toxicología ha desplegado una variedad de subdisciplinas como la toxicología clínica, la forense, la alimentaria, la industrial y la ambiental, que se preocupan por la protección de la salud pública a través de una mejor comprensión de los efectos nocivos de las sustancias que nos rodean cotidianamente, lo cual es necesario para mantener el bienestar humano y ambiental de las futuras generaciones.
La investigación toxicológica se ha desarrollado rápidamente para dar cabida a los especialistas en el estudio de fenómenos tóxicos en distintos niveles de organización biológica. Así, es posible determinar cómo las sustancias nocivas atacan macromoléculas como el ADN o las proteínas, para formar especies anormales que son promotores de respuestas patológicas. Estos nuevos avances proporcionan una base sólida para el progreso venidero en el sector de la investigación científica farmacológica.
Las distintas fases utilizadas en el estudio toxicológico de un fármaco o de una vacuna, son necesarias para evitar casos te toxicidad por medicamento, como el que ocurrió con la talidomida®. Es por eso, que resaltamos la importancia del tiempo, de los animales de laboratorio, pacientes, equipo y recursos humanos, que se requieren para realizar la toxicología de un agente terapéutico y lo esencial que es en estos procedimientos.
QFB. Grecia Elena Hurtado Núñez, Estudiante del Programa Institucional de Maestría en Ciencias Biológicas, Área de Biotecnología Alimentaria en la Facultad de Químico Farmacobiología de la Universidad Michoacana de San Nicolás de Hidalgo.
Esta dirección de correo electrónico está siendo protegida contra los robots de spam. Necesita tener JavaScript habilitado para poder verlo.
D.C. Martha Estrella García Pérez, Profesora investigadora del Instituto de Investigaciones Químico Biológicas de la Universidad Michoacana de San Nicolás de Hidalgo.
Esta dirección de correo electrónico está siendo protegida contra los robots de spam. Necesita tener JavaScript habilitado para poder verlo.
