
¿Qué son los virus?
Los médicos de la Roma antigua usaron el término “virus” para referirse a un veneno de origen animal de naturaleza desconocida. El refinamiento de los microscopios, logrado en los siglos XVIII y XIX, permitió la observación de diversos microorganismos, entre ellos las bacterias (ver Saber Más 21:11-16). A mediados del siglo XIX, con los primeros estudios formales de la microbiología, las bacterias fueron reconocidas como los agentes responsables de muchas enfermedades contagiosas (como la difteria y la tifoidea); así, esos microorganismos se consideraron como los virus de tales padecimientos. Los microbiólogos pioneros pensaban que las formas de vida más pequeñas del mundo microbiano eran las bacterias.
Para fines del siglo XIX, los microbiólogos habían reportado la existencia de varios agentes infecciosos de un tamaño mucho menor que el de las bacterias, ya que eran capaces de atravesar ciertos filtros que no permitían el paso de las células bacterianas; a dichos agentes “invisibles” se les llamó “Virus Filtrables”. De esta forma, se descubrieron virus que infectaban a plantas o animales y, más adelante, virus de hongos y de protozoarios. Poco a poco, en el ámbito biomédico se fueron distinguiendo los términos “bacterias” y “virus” como entidades claramente distintas. Sin embargo, la naturaleza de los enigmáticos virus permaneció todavía desconocida durante varios años más.
Descubrimiento de los bacteriófagos
En 1915, el microbiólogo inglés Frederick Twort hizo un descubrimiento muy importante. Encontró que cierto agente filtrable era capaz de matar a los estafilococos, un tipo de bacteria que él estudiaba, pero concluyó que dicho agente podría ser un tipo de enzima (o toxina) que la bacteria segregaba al medio y que tenía una actividad nociva sobre el microorganismo. Sólo como una hipótesis alterna, Twort consideró que el agente letal podría ser un tipo de virus. Estos hallazgos, desgraciadamente, se publicaron en una revista biomédica en forma de una breve nota y no llamaron la atención de la comunidad científica internacional. Poco después, Twort, que era médico militar, se enlistó en el ejército Británico para participar en la Primera Guerra Mundial, y aunque eventualmente regresó a su laboratorio, ya no volvió a trabajar con los virus.
En 1910, el microbiólogo franco-canadiense Félix d´Herelle se encontraba en Mérida, Yucatán, estudiando las plagas de la langosta. Observó que en las cajas de cultivo de una bacteria que infectaba a esos insectos, se formaban unas “placas” claras que parecían indicar zonas donde los microorganismos habían muerto. Intrigado, a su regreso a Francia, d’Herelle retomó el asunto, ahora con bacterias aisladas de las heces de enfermos de disentería (un trastorno gastrointestinal). En 1917, anunciaba triunfal el descubrimiento de un “microbio invisible” que destruía a la bacteria causante de la enfermedad, acuñando entonces el término “Bacteriófago” (del griego, “que come bacterias”) para este agente letal, y postuló que se trataba de un virus filtrable que era capaz de infectar, reproducirse y matar a las bacterias.
Y, sin embargo, se reproducen
Como ha ocurrido con frecuencia con los descubrimientos vanguardistas, la audaz propuesta de d´Herelle no fue aceptada de inmediato por los microbiólogos, lo cual retrasó algunos años el estudio de los bacteriófagos por otros científicos. Mientras tanto, d’Herelle siguió trabajando en el laboratorio con sus novedosos “bichitos” y estableció la metodología para obtenerlos a partir de cultivos bacterianos infectados en grandes cantidades… aunque sin poder verlos.
A pesar de que d’Herelle no concluyó sus estudios universitarios formales, fue nominado varias veces al premio Nobel, aunque nunca lo obtuvo. Sin embargo, apareció en un listado de la Fundación Nobel que incluye a científicos que se considera debieron haber recibido el premio en su tiempo. En 1949 d’Herelle falleció, pero debido a que las reglas de la Fundación impiden que el galardón sea otorgado en forma póstuma, tampoco le se le dio reconocimiento a sus méritos después de su muerte.
A principios de la década de 1930, el microbiólogo inglés Max Schlesinger, usando las técnicas de d’Herelle, aisló y purificó los bacteriófagos y demostró que estaban formados de ácidos nucleicos y proteínas en partes iguales. También encontró que estos virus se unen en forma específica a las bacterias antes de matarlas y originar la descendencia viral. Los hallazgos de Schlesinger mostraron, en forma contundente, que los bacteriófagos son entidades biológicas capaces de reproducirse y no simples estructuras químicas nocivas para las bacterias, tal como lo había predicho d’Herelle años atrás.
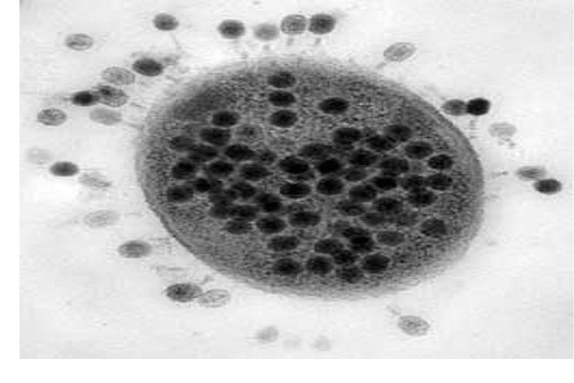
Célula bacteriana infectada por fagos. Se muestran, en la parte exterior, algunos virus o las cubiertas virales vacías y “nuevos” virus en el interior celular
El “Grupo de los Fagos”
Una vez establecida la capacidad reproductiva de los bacteriófagos, la siguiente pregunta constituía un reto intelectual formidable: ¿Cuál es el mecanismo mediante el cual ocurre el fenómeno de la infección viral? Afortunadamente, esta interrogante atrajo a algunas de las mentes más brillantes de ese tiempo, no solo microbiólogos y médicos, sino también algunos físicos. Este grupo de notables científicos, trabajando principalmente en universidades de EE. UU., abordó el estudio de los bacteriófagos, que abreviaron, a mediados de la década de 1930, como “Fagos”. Max Delbruck y Salvador Luria, junto con otros investigadores, formaron el llamado “Grupo de los Fagos” y realizaron los primeros experimentos dirigidos a dilucidar el mecanismo de la infección viral.
En 1939, este Grupo dilucidó el ciclo de vida de los fagos. Habían encontrado que, durante la infección de las bacterias, los fagos primero desaparecían de los cultivos y, después de 20 minutos aparecían, no un fago, sino cientos de ellos, al tiempo que ocurría la lisis (muerte) de las bacterias. Pero, para comprender cabalmente el ciclo de infección, faltaba un detalle…
¡Los genes del fago están en su ADN!
A mediados del siglo XX no se sabía cuál era la naturaleza química de los genes. Aunque, en 1944, en EE. UU., el grupo de Oswald Avery había reportado que los genes bacterianos parecían estar contenidos en su ácido desoxirribonucleico (ADN). Esta noción revolucionaria, sin embargo, no era aún aceptada, o incluso conocida, por la mayoría de la comunidad científica internacional de la época.
El hallazgo más trascendental para entender la estrategia de la infección por los fagos, fue el reportado en 1952 por los investigadores norteamericanos Alfred Hershey y Martha Chase. Este fue uno de los primeros experimentos biológicos en los que se emplearon Isótopos Radioactivos (formas inestables de los elementos químicos que emiten radiación, por la cual pueden ser “rastreados”). Utilizando isótopos del Azufre (35S) y del Fósforo (32P), Hershey y Chase encontraron que, durante el proceso de infección, solamente ingresa a la célula bacteriana el ADN del fago, quedando afuera de la bacteria la porción proteica, lo que significaba que la capacidad reproductiva del fago radicaba solamente en su ADN. Más adelante se encontró que las proteínas constituyen la cubierta del fago y sirven para proteger el ADN. Dicha cubierta es, además, la responsable de que el fago se adhiera a la superficie bacteriana. De esta forma, se concluyó que el ADN constituye el Genoma (conjunto de genes) que le permite al fago originar una descendencia de “nuevos” virus. Junto con el trabajo del grupo de Avery, este impactante hallazgo demostró, ahora sin lugar a dudas, que los genes de las bacterias y los fagos están constituidos por su ADN.
La revelación del mecanismo de la infección por los fagos estimuló de manera crucial el trabajo de James Watson y Francis Crick, que resultó en la dilucidación de la estructura de Doble Hélice del ADN en 1953. A la postre, esto condujo a una de las más grandes revoluciones de las ciencias biológicas.
¿Y, cómo es él?
Después de casi 25 años de haberse descubierto, los fagos seguían siendo un misterio: nadie los había “visto” (de hecho, ni algún tipo de virus). A principios de la década de 1940, en plena Segunda Guerra Mundial, se produjeron las primeras fotografías de los fagos. Este espectacular logro científico se alcanzó gracias al invento del poderoso microscopio electrónico. Es de hacer notar que el avance en estos trabajos sólo fue posible por las colaboraciones entre investigadores de bandos contrarios. Así, Helmut Ruska, en Alemania, y S. Luria, en EE. UU., reportaron las imágenes pioneras de los fagos.
Las fotografías los mostraron como unas estructuras fascinantes, formadas por una cabeza esférica o icosaédrica (llamada “cápside”) y una “cola” que tenía en un extremo fibras filamentosas como “patas”. Aunque más adelante se encontró que muchos fagos tienen formas diferentes, durante varios años la imagen de estos fotogénicos “módulos lunares” dominó la escena del mundo microbiano.
El microscopio electrónico reveló que los fagos son nanopartículas, esto es, estructuras del orden de millonésimas de milímetro, con tamaños que van de 20 a 100 nanómetros. Así, los fagos son 20 a 50 veces más pequeños que las bacterias que infectan y son, por lo tanto, invisibles a los microscopios convencionales. El material genético de los fagos puede ser muy sencillo, con menos de 10 genes, o más complejo, con más de 100 genes (una bacteria típica tiene unos 4 000 genes).

Proceso de infección bacteriana por los fagos

El mortífero ciclo de infección
Los hallazgos de los microbiólogos y los genetistas, junto con los trabajos sobre la ultraestructura viral, permitieron entender con gran detalle, a mediados del siglo XX, el mecanismo de infección bacteriana por los fagos. El ciclo de infección se puede resumir en los pasos que se describen en el siguiente esquema.
En 1969, M. Delbruck, S. Luria y A. Hershey obtuvieron el premio Nobel por “sus estudios sobre los mecanismos de la replicación y la estructura genética de los virus”.
Pero, ¿Están vivos?
Como se indicó en párrafos anteriores, por su simplicidad los fagos requieren de la maquinaria metabólica de la bacteria que infectan para expresar sus genes. Sólo así pueden multiplicarse y causar la lisis bacteriana. En ausencia de dicha célula hospedera, los fagos se comportan como entidades inertes, incapaces de reproducirse por sí mismos. Así, por ejemplo, una suspensión de fagos preparada en un laboratorio puede almacenarse en refrigeración por largos períodos de tiempo en forma latente. Estos fagos, sin embargo, no pierden su capacidad destructora cuando se ponen en contacto con las bacterias que infectan; por esta razón, los fagos son considerados como un tipo de “Parásitos Genéticos”. Puede decirse que se encuentran en una fase intermedia entre la materia viva y la materia inerte.
No siempre son tan malvados
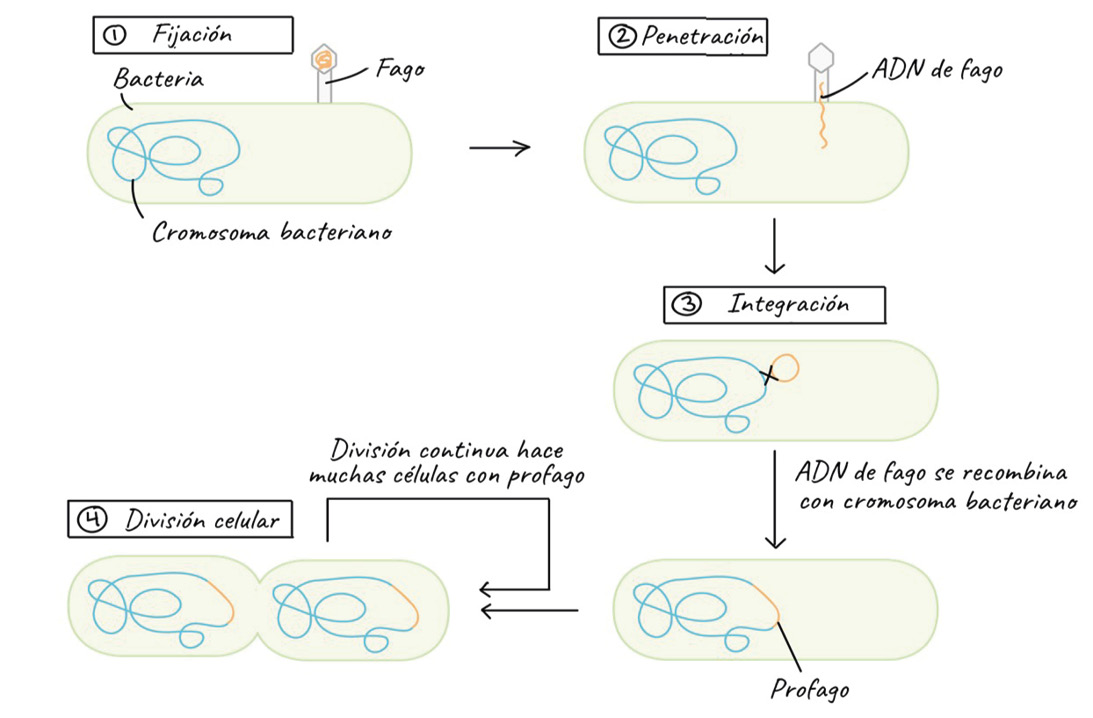
A fines de la década de 1940, ya concluida la Segunda Guerra Mundial, el científico francés André Lwoff encontró que los fagos no siempre son tan terribles como parecen. Empleando cultivos bacterianos, Lwoff descubrió los llamados fagos “Temperados” o “Moderados”, los cuales infectan a sus bacterias hospederas pero no las matan, en un fenómeno llamado “Lisogenia”. Siguiendo los primeros pasos del ciclo de infección, los fagos temperados inyectan a la bacteria su pequeño genoma, pero éste, en lugar de reproducirse, se integra al enorme genoma bacteriano. De esta manera, en la lisogenia los genes del fago pasan a formar parte del material genético de la célula hospedera y se heredan a sus descendientes durante la división celular. Esta forma latente del fago fue llamada por Lwoff como “Profago”.
En la actualidad, se ha reportado que más del 80% de los fagos son temperados, esto es, la gran mayoría no causan la muerte de las bacterias que infectan. Esto sugiere que la lisogenia es una estrategia evolutiva que favorece la supervivencia de los fagos, perpetuando sus genomas en las diversas poblaciones bacterianas.
Transferencia de genes por los fagos
Aunque la lisogenia generalmente es una propiedad estable, bajo determinadas condiciones puede revertirse, por ejemplo, en situaciones que ponen en riesgo la supervivencia bacteriana. En este caso, ocurre la “Inducción”: el ADN del profago sale de su latencia, se escinde del genoma bacteriano y lleva a cabo el ciclo de infección propio de un virus activo, proceso que culmina con la muerte celular; sin embargo, la escisión del ADN del profago durante la inducción, no siempre es un fenómeno preciso ya que con frecuencia el genoma viral “acarrea” genes bacterianos al separarse del genoma de la célula hospedera y estos genes pueden ser transmitidos a otras bacterias en posteriores ciclos de lisogenia (fenómeno llamado “Transducción”). Los “nuevos” genes pueden ahora dotar de atributos benéficos a las bacterias receptoras como la adquisición de propiedades de virulencia, resistencia a antibióticos, e incluso pueden originar enzimas del metabolismo bacteriano. Se ha considerado que los genes transportados por los fagos temperados constituyen ¡la mayor reserva de información genética de la Tierra!
Por su pequeño tamaño, los genomas de los fagos se emplearon como eficientes vehículos de clonación en el nacimiento de la Ingeniería Genética a principios de la década de 1970. Hasta la fecha, se utilizan ampliamente para la manipulación genética y la transferencia de genes de un organismo a otro.
 Los fagos y los ecosistemas terrestres
Los fagos y los ecosistemas terrestres
Los fagos se localizan en el suelo, en las plantas y en el intestino de los animales, pero en el ambiente donde se encuentran en mayor cantidad es en los océanos, los cuales constituyen “hervideros” de fagos, no solo en los mares templados, sino también en los gélidos océanos Ártico y Antártico, e incluso en los inhóspitos sedimentos marinos. Se ha encontrado que existen entre diez mil millones y un billón (1010-1012) de partículas virales por cada litro de agua de mar. La cantidad de fagos calculada para todo el planeta arroja una cifra fantástica: 1031 (un diez seguido de 31 ceros), cantidad varias veces mayor que ¡el número de galaxias que se predice que existen en el Universo!
Se estima que, en un solo día, 20-40 % de las bacterias presentes en los mares son destruidas por los fagos. Ante este terrible efecto depredador, surge la pregunta ¿Por qué no han desaparecido por completo las bacterias marinas? La respuesta es que, entre la población, continuamente se seleccionan al azar bacterias resistentes, generándose así mutantes bacterianas que ya no son destruidas por los fagos.
En los ambientes marinos, la avasalladora destrucción de las bacterias por los fagos libera sus componentes orgánicos (azúcares, lípidos, aminoácidos, etc.), proceso que representa una parte importante del Reciclaje Global de Carbono. Este reciclaje, a su vez, afecta la cantidad de oxígeno que se transfiere de los mares a la atmósfera, en intercambio con el dióxido de carbono (CO₂) del aire. Se postula que la vida microbiana de los océanos absorbe la mitad de las emisiones de CO₂ generadas en el planeta. Así, la infección por los fagos influye directamente en las condiciones climáticas de la Tierra, al alterar el desarrollo de las bacterias del fitoplancton marino, considerado como uno de los “pulmones” más importantes de la Tierra. Todos estos cambios, provocados por los diminutos, aunque abundantísimos fagos, pueden también modificar los niveles oceánicos de nutrimentos, los cuales son esenciales para mantener las redes alimentarias marinas, así como para determinar la abundancia o escasez de los recursos pesqueros a nivel global.
El futuro de los fagos
Por falta de espacio, se han dejado fuera algunos tópicos relevantes de los fagos, que sin duda merecerían un artículo aparte. Uno de ellos es la utilización de los fagos en aspectos médicos: por ejemplo, el empleo de fagos en el tratamiento de infecciones bacterianas (tema propuesto hace casi un siglo por d´Herelle), se presenta en el artículo siguiente de este número. Otro tema es el uso de fagos para el desarrollo de anticuerpos contra ciertas enfermedades, cuyos promotores, los científicos George Smith y Gregory Winter, obtuvieron el premio Nobel en 2018.
Se puede concluir que, además de las relevantes aportaciones con que los fagos contribuyeron al desarrollo de las ciencias biológicas en el pasado, se avizoran nuevos descubrimientos y aplicaciones futuras resultantes del estudio de estos maravillosos virus bacterianos.
Bacteriófagos. http://www.microinmuno.qb.fcen.uba.ar/SeminarioBacteriofagos.htm
Cervantes C. (2015). El maravilloso mundo de las bacterias. Saber Más, 21:11-16. https://www.sabermas.umich.mx/archivo/articulos/165-numero-219/325-el-maravilloso-mundo-de-las-bacterias.html
Mayer G. (2015). Bacteriología. Capítulo siete. Bacteriófagos. Microbiology and Immunology On-line (Hunt, R.C. Ed.).
https://www.microbiologybook.org/Spanish/chapter7.htm
Carlos Cervantes, Profesor e Investigador del Laboratorio de Microbiología en el Instituto de Investigaciones Químico-Biológicas de la Universidad Michoacana de San Nicolás de Hidalgo.
Esta dirección de correo electrónico está siendo protegida contra los robots de spam. Necesita tener JavaScript habilitado para poder verlo.
